Ауыр туа біткен С протеинінің тапшылығы (АТБСПТ) — бұл сирек кездесетін аутосомды-рецессивті ауру, бастапқы өлім-жітімнің жоғары болуына және тірі қалғандарда ұзақ мерзімді асқынулардың дамуына әкеледі1. АТБСПТ - аса сирек ауру, аурушаңдық жиілігі тірі туылған нәрестеге шаққанда 1:4 000 000-нан 1:500 000-ға дейін2,9.
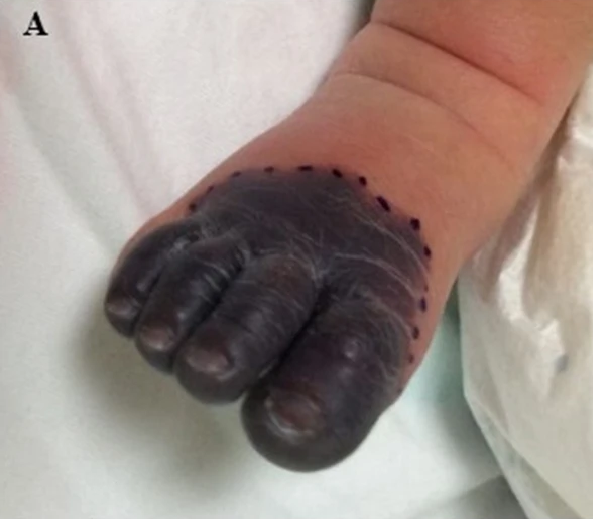
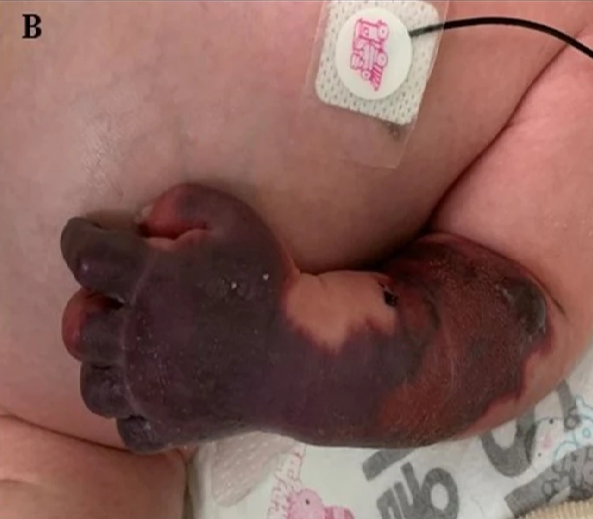
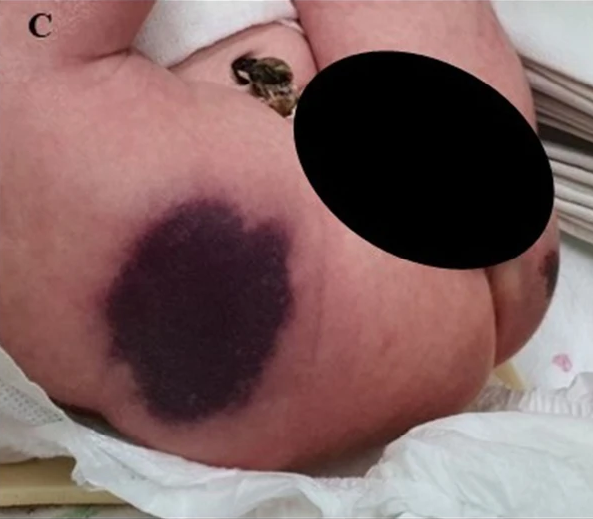
Жаңа туған нәрестелерде АТБСПТ туғаннан кейін алғашқы сағаттардың ішінде-ақ тері некрозымен жүретін жедел пурпура түрінде, диссеминацияланған тамырішілік ұюмен, артериялық және көктамырлық тромбоз түрінде байқалуы мүмкін3.
Терідегі зақымданулар тез үдеп, дұрыс емес пішінге еніп, көкшіл‑қара түсті геморрагиялық некроз ошақтарына айналады4.
Неонаталдық кезеңнен кейін АТБСПТ инфекция немесе жарақатпен қоздырылатын жедел пурпураның келесі эпизодтарын және қайталанатын көктамырлық тромбоздық оқиғаларды, соның ішінде терең көктамыр тромбозын (ТКТ) және өкпе артериясының тромбоэмболиясын (ӨАТЭ)3 тудыруы мүмкін.
Song U, Ryu YH, Hong K, et al. Severe protein C deficiency in a newborn caused by a homozygous pathogenic variant in the PROC gene: a case report. BMC Pediatr. 2021;21(1):453. Published 2021 Oct 16. doi:10.1186/s12887-021-02923-610.
АТБСПТ-ны ерте тану және емдеу өлім-жітімді төмендету және денсаулыққа ұзақ мерзімді салдардың алдын алу үшін шешуші мәнге ие3.
С протеинінің маңызы қандай?5
С протеині —
K-витаминіне тәуелді табиғи антикоагулянт, қанның ұю каскадының маңызды құрамдас бөлігі. Оның негізгі қызметі — коагулянт тромбиннің белсенділігін реттеу; оның активациясы фибриннің түзілуіне және қанның ұюына әкеледі.
С протеинінің қосымша әсерлері:
- жанама профибринолитикалық әсер (яғни тромбтың ыдырауына ықпал етеді): плазминоген активаторының тежегіші-1 (PAI-1)мен байланысу арқылы тіндік плазминоген активаторының (tPA) белсенділігін арттырады
- қабынуға қарсы және цитопротективті әсер
Ауыр туа біткен С протеинінің тапшылығы (АТБСПТ) С протеинінің туа біткен тапшылығының бір түрі болып табылады және С протеинінің геніндегі мутациялармен (PROC) байланысты; ол 2-хромосомада (q13-14 аймағы) орналасқан.
АТБСПТ PROC геніндегі гомозиготалы және құрама гетерозиготалы мутация жағдайларын қамтиды4.
Сонымен қатар, жоғарыда көрсетілген әр генотиптің ішінде екі қосалқы түрі ажыратылады6:
1-ТИП — С протеинінің концентрациясы да, оның белсенділігі де төмендейді
2-ТИП — С протеинінің концентрациясы қалыпты, ал белсенділігі төмен
АТБСПТ кезінде С протеинінің деңгейі іс жүзінде болмайды [ПС < 1 ХБ/дл (10%)]4.
АТБСПТ-ның клиникалық белгілері
АТБСПТ-ның клиникалық белгілері әдетте туғаннан кейінгі алғашқы сағаттар ішінде пайда болады3:
Жылдам үдейтін молниенос
пурпура (МП).
Диссеминацияланған тамырішілік ұю (ДТІҰ).
Неврологиялық асқынулар: ми веналарының тромбозы нәтижесінде дамитын екіншілік перивентрикулярлық инсульт және гидроцефалиямен сипатталады
Соқырлық: шынытәрізді денеге қан құйылуы немесе торқабық венасының, торқабық артериясының не шынытәрізді дене венасының тромбозы салдарынан, торқабықтың ажырауымен қатар дамуы мүмкін; бұл лейкокориямен немесе көру жүйкесінің ишемиялық атрофиясымен көрініс береді
Ауыр туа біткен С протеинінің тапшылығы диагнозын келесі әдістердің үйлесімі арқылы растауға болады:
02
S протеинінің деңгейін анықтау7
03
С протеинінің антигенін анықтау1
S протеинінің деңгейі қалыпты болғанда С протеинінің төмен деңгейі ауыр туа біткен С протеинінің тапшылығын көрсетеді7.
Сау жаңа туған нәрестелерде С және S протеиндерінің деңгейі ересектерге қарағанда едәуір төмен екенін ескеру маңызды3.
Дифференциалды диагностика және асқынуларды анықтау үшін:
01
Қанның жалпы талдауы (гемоглобин, лейкоциттер, тромбоциттер)8
04
Протромбин уақыты (ПВ)8
05
Белсендірілген ішінара тромбопластин уақыты (АчТВ)8
07
Ата-аналардағы С протеинінің деңгейін зерттеу (С протеинінің белсенділігін және С протеинінің антиген концентрациясын бағалау)1
08
МРТ (ми веналары тромбозын бар-жоғын анықтау үшін)3
09
Офтальмологтың кеңесін алу3
МАҢЫЗДЫ: АТБСПТ-ны ерте тану және емдеу денсаулыққа ұзақ мерзімді салдардың алдын алу және өлім-жітімді төмендету үшін шешуші мәнге ие3.
Дереккөздер:
- Chalmers E, Cooper P, Forman K, et al. Purpura fulminans: recognition, diagnosis and management. Arch Dis Child. 2011;96(11):1066-1071. doi:10.1136/adc.2010.199919.
- Goldenberg NA, Manco-Johnson MJ. Protein C deficiency. Haemophilia. 2008;14(6):1214-1221. doi:10.1111/j.1365-2516.2008.01838.x.
- Price VE, Ledingham DL, Krümpel A, Chan AK. Diagnosis and management of neonatal purpura fulminans. Semin Fetal Neonatal Med. 2011;16(6):318-322. doi:10.1016/j.siny.2011.07.009.
- Knoebl PN. Severe congenital protein C deficiency: the use of protein C concentrates (human) as replacement therapy for life-threatening blood-clotting complications. Biologics. 2008;2(2):285-296. doi:10.2147/btt.s1954.
- Bouwens EA, Stavenuiter F, Mosnier LO. Mechanisms of anticoagulant and cytoprotective actions of the protein C pathway. J Thromb Haemost. 2013;11 Suppl 1(01):242-253. doi:10.1111/jth.12247.
- Minford A, Brandão LR, Othman M, et al. Diagnosis and management of severe congenital protein C deficiency (SCPCD): Communication from the SSC of the ISTH. J Thromb Haemost. 2022;20(7):1735-1743. doi:10.1111/jth.15732.
- Libourel EJ, Meinardi JR, de Kam PJ, et al. Protein C/S ratio, an accurate and simple tool to identify carriers of a protein C gene mutation. Br J Haematol. 2002;118(2):615-618. doi:10.1046/j.1365-2141.2002.03597.x.
- Khor B, Van Cott EM. Laboratory tests for protein C deficiency. Am J Hematol. 2010;85(6):440-442. doi:10.1002/ajh.21679.
- Orphanet (2009). Severe hereditary thrombophilia due to congenital protein C deficiency. Accessed December 26, 2025. https://www.orpha.net/en/disease/detail/745
- Song U, Ryu YH, Hong K, et al. Severe protein C deficiency in a newborn caused by a homozygous pathogenic variant in the PROC gene: a case report. BMC Pediatr. 2021;21(1):453. Published 2021 Oct 16. doi:10.1186/s12887-021-02923-6
VV-MEDMAT-131320
2026 жыл, қаңтар айы